Sfondate è Cuncepimentu di Studiu
Retatrutide (LY3437943) hè una nova droga à peptide unicu chì attivatrè recettori simultaneamenteGIP, GLP-1 è glucagonu. Per valutà a so efficacia è a so sicurezza in l'individui cun obesità ma senza diabete, hè statu realizatu un studiu di fase 2, aleatoriu, in doppio cieco, cuntrullatu da placebo (NCT04881760). Un totale di338 participanticù un BMI ≥30, o ≥27 cù almenu una comorbidità ligata à u pesu, sò stati randomizzati per riceve placebo o retatrutide (1 mg, 4 mg cù dui schemi di titolazione, 8 mg cù dui schemi di titolazione, o 12 mg) amministrati una volta à settimana per iniezione sottocutanea per 48 settimane. Uendpoint primariuera u cambiamentu percentuale di u pesu corpurale à 24 settimane, cù endpoints secundarii chì includenu u cambiamentu di pesu à 48 settimane è i limiti di perdita di pesu categurichi (≥5%, ≥10%, ≥15%).
Risultati Chjave
-
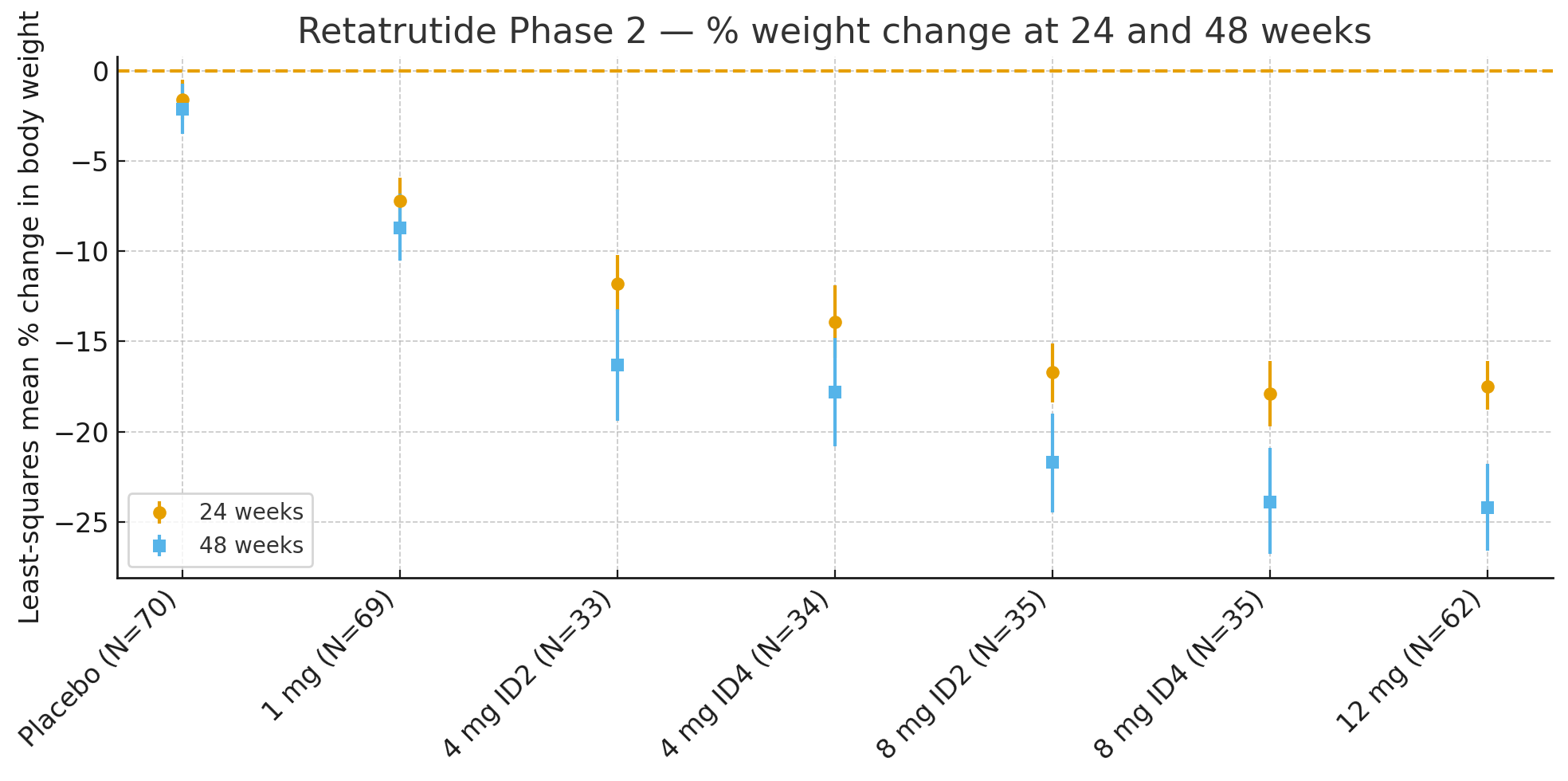
24 settimaneA media di i minimi quadrati di u cambiamentu percentuale di u pesu corpurale in relazione à u livellu di basa era
-
Placebo: −1,6%
-
1 mg: −7,2%
-
4 mg (cumminati): −12,9%
-
8 mg (cumminati): −17,3%
-
12 mg: −17,5%
-
-
48 settimane: U cambiamentu percentuale di u pesu corpurale era
-
Placebo: −2,1%
-
1 mg: −8,7%
-
4 mg (cumminati): −17,1%
-
8 mg (cumminati): −22,8%
-
12 mg: −24,2%
-
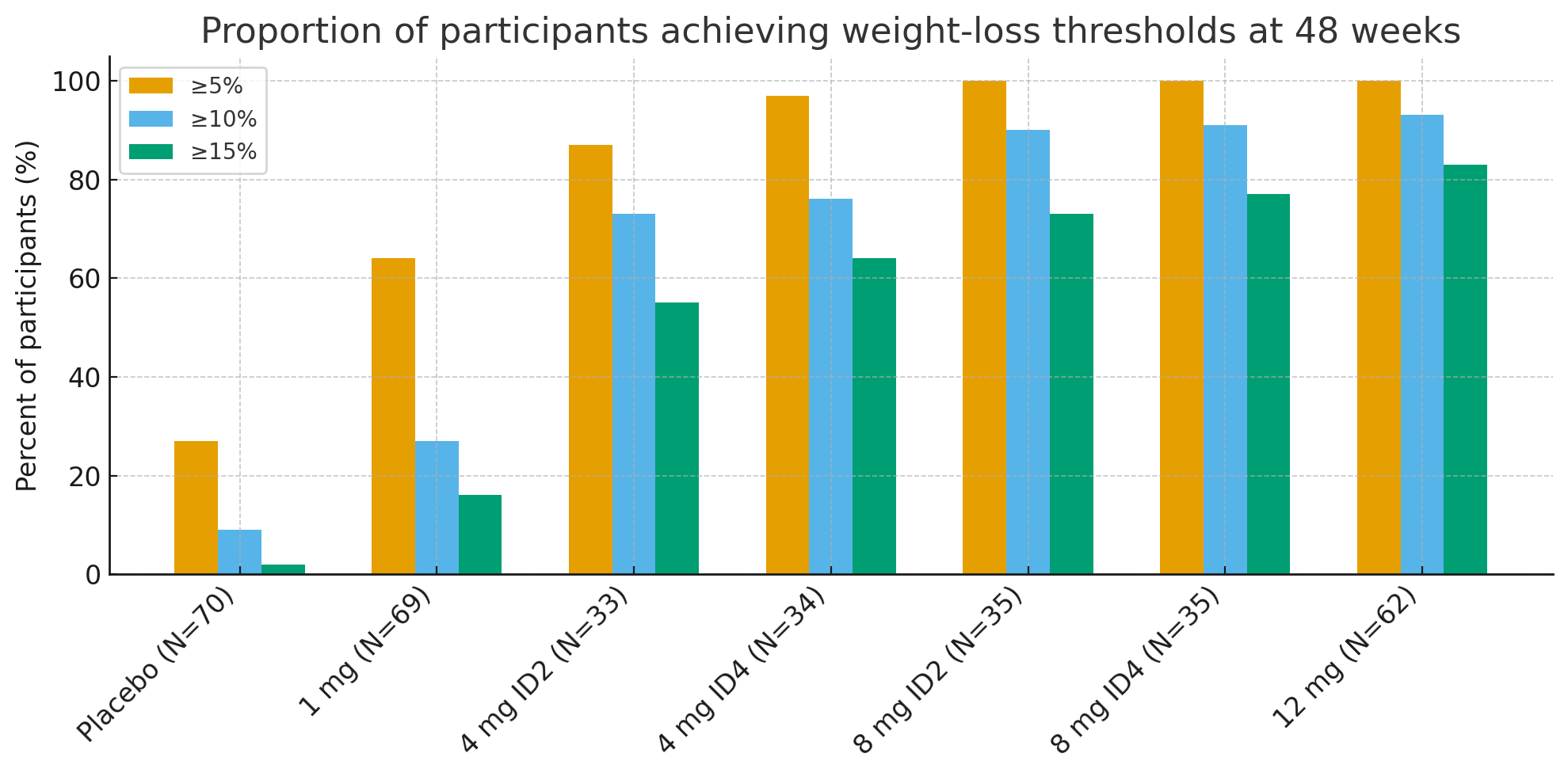
À 48 settimane, e proporzioni di participanti chì anu righjuntu limiti di perdita di pesu clinicamente significativi eranu sorprendenti:
-
Perdita di pesu ≥5%: 27% cù placebo vs. 92–100% in gruppi attivi
-
≥10%: 9% cù placebo vs. 73–93% in gruppi attivi
-
≥15%: 2% cù placebo vs. 55–83% in gruppi attivi
In u gruppu di 12 mg, finu à26% di i participanti anu persu ≥30% di u so pesu di basa, una magnitudine di perdita di pesu paragunabile à a chirurgia bariatrica.
Sicurezza
L'effetti avversi i più cumuni eranu gastrointestinali (nausea, vomitu, diarrea), generalmente da lievi à moderati è correlati à a dose. Dosi iniziali più basse (titrazione di 2 mg) anu riduttu questi effetti. Aumenti di a frequenza cardiaca correlati à a dose sò stati osservati, cù un piccu à a settimana 24, poi diminuendu. I tassi di discontinuazione variavanu da 6 à 16% in i gruppi attivi, un pocu più alti di u placebo.
Cunclusioni
In adulti cun obesità senza diabete, a retatrutide sottucutanea settimanale per 48 settimane hà prudutturiduzioni sustanziali è dipendenti da a dose di u pesu corpurale(finu à ~24% di perdita media à a dosa più alta), accumpagnata da miglioramenti in i marcatori cardiometabolici. L'eventi avversi gastrointestinali eranu frequenti ma gestibili cù a titolazione. Questi risultati di fase 2 suggerenu chì a retatrutide puderia rapprisintà un novu benchmark terapeuticu per l'obesità, in attesa di cunferma in studii di fase 3 più ampi è à longu andà.
Data di publicazione: 28 di settembre di u 2025